核準日期:2022年01月30日
修改日期:
鹽酸左西替利嗪口服溶液說明書
請仔細閱讀說明書并在醫師指導下使用
【藥品名稱】
通用名稱:鹽酸左西替利嗪口服溶液
英文名稱:Levocetirizine Dihydrochloride Oral Solution
漢語拼音:Yansuan Zuoxitiliqin Koufurongye
【成份】
本品主要成份為鹽酸左西替利嗪。
化學名稱:(R)-[2-[4-[(4-氯苯基)苯甲基]-1-哌嗪基]-乙氧基]乙酸二鹽酸鹽
化學結構式:
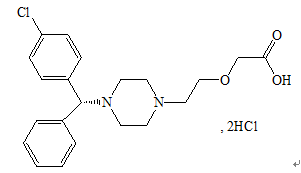
分子式:C21H25ClN2O3·2HCl
分子量:461.81
【性狀】
本品為無色的澄清液體。
【適應癥】
蕁麻疹、過敏性鼻炎、濕疹、皮炎、皮膚瘙癢癥等。
【規格】
0.05%(150ml︰75mg)
【用法用量】
12歲及以上青少年和成人:每晚一次,每次5mg(10ml)。某些患者可每晚一次,每次2.5mg(5ml)。
6~11歲兒童:每晚一次,每次2.5mg(5ml)。
6個月~5歲兒童:每晚一次,每次1.25mg(2.5ml)。
12歲及以上青少年和成人肝腎功能損害患者的劑量調整:
l輕度腎功能損害者(肌酐清除率CLCR=50~79ml/min):每日一次,每次2.5mg(5ml)。
l中度腎功能損害者(CLCR=30~49ml/min):每隔一日一次,每次2.5mg(5ml)。
l嚴重腎功能損害者(CLCR=10~29ml/min):每周2次(平均每3~4日一次),每次2.5mg(5ml)。
l腎病晚期患者(CLCR<10ml/min)和正在透析患者,不得服用本品。
11歲以下腎功能損害兒童患者禁用。
僅肝功能損害者不用調整劑量,同時肝、腎功能損害者推薦調整劑量。
本品可與食物同服,也可單獨服用。
【不良反應】
嗜睡、疲勞、乏力和尿潴留與鹽酸左西替利嗪應用相關。
1.臨床試驗經驗
在14項為期1周至6個月的對照臨床試驗中,2708例暴露于左西替利嗪的過敏性鼻炎和慢性特發性蕁麻疹患者顯示出下述安全性數據。
成人和青少年的短期(暴露時間達6周)安全性數據是基于8項涉及1896例患者(男性825例、女性1071例)用左西替利嗪每晚一次,每次2.5、5mg等治療的臨床試驗。
兒科患者的短期安全性數據是基于2項涉及243例患有過敏性鼻炎的兒童(6~12歲的男性162例、女性81例)用左西替利嗪治療4至6周的臨床試驗,一項114例患有過敏性鼻炎或慢性特發性蕁麻疹的兒童(1~5歲的男性65例、女性49例)用左西替利嗪治療2周的臨床試驗,和一項45例患有過敏性鼻炎或慢性蕁麻疹癥狀的兒童(6~11個月的男性28例、女性17例)用左西替利嗪治療2周的臨床試驗。
成人和青少年的長期(暴露4或6個月)安全性數據是基于2項涉及428例過敏性鼻炎患者(男性190例、女性238例)用左西替利嗪每日一次、每次5mg治療的臨床試驗。一項涉及255例12~24個月患者用左西替利嗪治療18個月的臨床試驗也提供了長期安全性數據。
因為臨床試驗是在各種條件下進行的,一種藥物在各臨床試驗所觀察到的不良反應發生率不能直接與另一種藥物在一項臨床試驗中的發生率相比較,也不能反映實踐中觀察到的發生率。
12歲及以上青少年和成人
在為期6周的試驗中,成人和青少年患者的平均年齡為32歲,44%為男性、56%為女性,絕大部分(超過90%)為白種人。
試驗中服用左西替利嗪2.5mg和5mg的試驗組分別有43%和42%的受試者至少有1例不良事件,而安慰劑組有43%。
在為期1至6周的安慰劑對照試驗中,最常見的不良反應為嗜睡、鼻咽炎、疲勞、口干和咽炎,多數程度為輕到中度。左西替利嗪引起的嗜睡隨試驗劑量2.5mg、5mg等排序,是導致中斷試驗(0.5%)的最常見不良反應。
表1列出8項安慰劑對照臨床試驗中12歲及以上受試者暴露于左西替利嗪2.5mg或5mg時報告的發生率超過或等于2%、同時比安慰劑組發生率高的不良反應。
表1.為期1至6周的安慰劑對照臨床試驗中12歲及以上受試者暴露于左西替利嗪每日一次、每次2.5mg或5mg時報告的≥2%的不良反應
不良反應 | 左西替利嗪2.5mg (n=421) | 左西替利嗪5mg (n=1070) | 安慰劑 (n=912) |
嗜睡 | 22(5%) | 61(6%) | 16(2%) |
鼻咽炎 | 25(6%) | 40(4%) | 28(3%) |
疲勞 | 5(1%) | 46(4%) | 20(2%) |
口干 | 12(3%) | 26(2%) | 11(1%) |
咽炎 | 10(2%) | 12(1%) | 9(1%) |
12歲及以上青少年和成人暴露于左西替利嗪時所見發生率高于安慰劑組的其他不良反應有昏厥(0.2%%)和體重增加(0.5%)。
6~11歲兒科患者
2項短期安慰劑對照、雙盲臨床試驗中共有243例6~11歲兒科患者服用左西替利嗪。患者平均年齡為9.8歲,6~8歲有79例(32%),50%為白種人。表2列出安慰劑對照臨床試驗中6~11歲受試者暴露于左西替利嗪時報告的發生率超過或等于2%、同時比安慰劑組發生率高的不良反應。
表2.為期4和6周的安慰劑對照臨床試驗中6~11歲受試者暴露于左西替利嗪時報告的≥2%的不良反應
不良反應 | 左西替利嗪 (n=243) | 安慰劑 (n=240) |
發熱 | 10(4%) | 5(2%) |
咳嗽 | 8(3%) | 2(<1%) |
嗜睡 | 7(3%) | 1(<1%) |
鼻出血 | 6(2%) | 1(<1%) |
1~5歲兒科患者
一項為期2周的安慰劑對照、雙盲安全性試驗中共有114例1~5歲兒科患者服用左西替利嗪。患者平均年齡為3.8歲,1~2歲占32%,71%為白種人、18%為黑人。表3列出安慰劑對照安全性試驗中1~5歲受試者暴露于左西替利嗪時報告的發生率超過或等于2%、同時比安慰劑組發生率高的不良反應。
表3.為期2周的安慰劑對照安全性試驗中1~5歲兒科受試者暴露于左西替利嗪時報告的≥2%的不良反應
不良反應 | 左西替利嗪 (n=114) | 安慰劑 (n=59) |
發熱 | 5(4%) | 1(2%) |
腹瀉 | 4(4%) | 2(3%) |
嘔吐 | 4(4%) | 2(3%) |
中耳炎 | 3(3%) | 0(0%) |
6~11個月兒科患者
一項為期2周的安慰劑對照、雙盲安全性試驗中共有45例6~11個月兒科患者服用左西替利嗪。患者平均年齡為9個月,51%為白種人、31%為黑人。安慰劑對照安全性試驗中6~11個月受試者暴露于左西替利嗪時報告的發生率超過1例(例如,≥3%受試者)、同時比安慰劑組發生率高的不良反應包括腹瀉和便秘,在左西替利嗪和安慰劑治療組分別各報告有6例(13%)和1例(4%)、3例(7%)和1例(4%)。
長期臨床試驗經驗
2項對照臨床試驗中,428例12歲及以上患者(男性190例、女性238例)用左西替利嗪每日一次、每次5mg治療4或6個月。患者特征與安全性特性與短期試驗中所見相似。10例患者(2.3%)因嗜睡、疲勞或乏力中斷試驗,與之相比,安慰劑組有2例(<1%)。
未進行12歲以下過敏性鼻炎或慢性特發性蕁麻疹兒科患者的長期臨床試驗。
實驗室檢查異常
臨床試驗中有<1%患者報告有血膽紅素和轉氨酶一過性升高,未導致任何患者中斷試驗。
2.上市后經驗
在臨床試驗期間報告的和上述所列的不良反應之外,左西替利嗪上市后也確認了不良反應。由不確定樣本量人群主動報告的不良反應,不可能確切估計其發生率或建立與藥物暴露量的因果關系。報告的不良反應有:超敏性和過敏反應、食欲增加、血管性水腫、固定性藥疹、瘙癢、皮疹和蕁麻疹、抽搐、感覺異常、頭暈、戰栗、味覺障礙、眩暈、運動障礙(包括肌張力失常和動眼危象)、易激惹和騷動、幻覺、抑郁、失眠、自殺意念、視覺紊亂、視力模糊、心悸、心動過速、呼吸困難、惡心、嘔吐、肝炎、排尿困難、尿潴留、肌痛、關節痛和水腫。
除了這些左西替利嗪治療時報告的反應,西替利嗪上市后經驗中也報告有其他可能的嚴重不良事件。因左西替利嗪是西替利嗪的主要活性成分,應考慮下述不良事件在左西替利嗪治療時有可能出現:口面運動障礙、嚴重低血壓、膽汁淤積、腎小球性腎炎、死胎、抽搐、肌痙攣、錐體外系癥狀和急性泛發性發疹性膿皰病(AGEP)。
【禁忌】
對左西替利嗪、西替利嗪或其他哌嗪類衍生物,以及本品其他輔料過敏者禁用。
腎病晚期患者(CLCR<10ml/min)和透析患者禁用。
11歲以下腎功能損害兒童患者禁用。
【注意事項】
1.嗜睡:臨床研究中報道鹽酸左西替利嗪治療時某些患者出現嗜睡、疲勞和乏力,從事危險職業、駕駛或操縱機器者應慎用。由于可能發生額外的警覺性降低以及對中樞神經系統性能的額外損害,應避免鹽酸左西替利嗪與酒精或其他中樞神經系統鎮靜劑合并使用。
2.尿潴留:鹽酸左西替利嗪上市后報道有尿潴留,有尿潴留發病誘因(如脊髓損傷、前列腺增生)的患者應慎用。出現尿潴留后應停用鹽酸左西替利嗪。
【孕婦及哺乳期婦女用藥】不適用。
【兒童用藥】
見【用法用量】。
【老年用藥】同成人。
【藥物相互作用】
體外數據說明左西替利嗪不可能通過抑制或誘導肝藥物代謝酶而產生藥代動力學相互作用。尚未進行左西替利嗪體內藥物相互作用的研究。消旋西替利嗪進行的藥物相互作用研究顯示:消旋西替利嗪與安替比林、偽麻黃堿、紅霉素、阿奇霉素、酮康唑和西咪替丁間無相互作用。400mg劑量的茶堿導致西替利嗪的清除率有較小的降低,可能是由于較高的茶堿劑量具有較強的效果。利托那韋增加西替利嗪的血漿AUC約42%,并伴有半衰期延長(53%)和清除率下降(29%),同時服用西替利嗪不能改變利托那韋的行為。
【藥物過量】
劑量過量時成人的癥狀可能包括嗜睡。在兒童起初可能出現焦慮或坐立不安,隨后嗜睡。本品無特效拮抗劑。一旦發生劑量過量,推薦對癥或支持性治療。左西替利嗪不能通過透析有效去除,除非同時服用一種可透析藥物。
左西替利嗪急性最高無毒劑量在小鼠為240mg/kg(按體表面積折算,約相當于成人臨床日推薦最大口服劑量的190倍、6~11歲兒童臨床日推薦最大口服劑量的230倍、6個月~5歲兒童臨床日推薦最大口服劑量的180倍),在大鼠為240mg/kg(按體表面積折算,約相當于成人臨床日推薦最大口服劑量的390倍、6~11歲兒童臨床日推薦最大口服劑量的460倍、6個月~5歲兒童臨床日推薦最大口服劑量的370倍)。
【藥理毒理】
左西替利嗪
藥理作用
本品為西替利嗪活性對映異構體,口服選擇性組胺H1受體拮抗劑。無明顯抗膽堿和抗5-羥色胺作用,中樞抑制作用較小。
毒理研究
遺傳毒性
左西替利嗪Ames試驗、人淋巴細胞染色體畸變試驗、小鼠淋巴瘤試驗和小鼠微核試驗結果均為陰性。
生殖毒性
大鼠和兔經口給予左西替利嗪劑量分別達到200和120mg/kg(按體表面積折算,分別約相當于成人臨床推薦最大日口服劑量的320和390倍),未見致畸性。
西替利嗪
生殖毒性
小鼠生育力和一般毒性試驗結果提示,西替利嗪經口給藥劑量達64mg/kg(按體表面積折算,約相當于成人臨床推薦最大日口服劑量的25倍)時,對生育力無損傷。
哺乳期小鼠(母鼠)經口給藥西替利嗪劑量達96mg/kg(按體表面積折算,約相當于成人臨床推薦最大日口服劑量的40倍)時,可引起仔鼠體重增長延遲。Beagle犬的研究表明,給藥量的大約3%經乳汁排泄。
致癌性
左西替利嗪未進行致癌性試驗,西替利嗪致癌性試驗可以評估左西替利嗪的潛在致癌性。大鼠連續2年經口給藥的致癌性試驗中,劑量達20mg/kg(按體表面積折算,約相當于成人或6個月至5歲兒童臨床推薦最大日口服劑量的15倍,或6~11歲兒童臨床推薦最大日劑量的10倍)時,未見致癌性。小鼠連續2年經口給藥的致癌性試驗中,劑量達16mg/kg(按體表面積折算,約相當于成人或6個月至5歲兒童臨床推薦最大日口服劑量的6倍,或6~11歲兒童臨床推薦最大日劑量的4倍)時,可引起雄性動物良性肝腫瘤的發生率增加;劑量為4mg/kg(按體表面積折算,約相當于成人或6個月至5歲兒童臨床推薦最大日口服劑量的2倍,或相當于6~11歲兒童臨床推薦最大日口服劑量)時,未見良性腫瘤發生率的增加。上述發現的臨床意義尚不清楚。
【藥代動力學】
在成年健康受試者中,左西替利嗪在治療劑量范圍內顯示線性藥代動力學特性,5mg口服溶液與5mg片劑間生物等效。左西替利嗪口服給藥后吸收迅速且完全。成年健康受試者服用鹽酸左西替利嗪口服溶液5mg后約0.5小時血藥濃度達到峰值。每日口服給藥的蓄積率為1.12,給藥2日后達穩態。單劑量服用5mg和每日單次服用5mg的峰濃度分別為270ng/ml和308ng/ml。左西替利嗪體外平均血漿蛋白結合率約91%~92%,表觀分布容積為0.4L/kg。左西替利嗪在人體內的代謝率小于給藥劑量的14%,因此基因多態性或合并服用肝酶抑制劑的影響可忽略。口服溶液給藥后,成人的血漿消除半衰期約8~9小時,全身清除率約0.63ml/kg/min。左西替利嗪及其代謝物主要經尿液排泄,腎清除率與肌酐清除率相關,腎功能損害者的左西替利嗪清除率下降。在吸收和清除的過程中左西替利嗪不會轉換為右西替利嗪。
兒科患者:14名6~11歲、體重20~40kg的兒童單劑量口服5mg左西替利嗪的兒科藥代動力學研究中,Cmax和AUC約為一項交叉比較研究中報道的成人數據的2倍多。平均Cmax為450ng/ml,平均達峰時間為1.2小時,體重標準化后,全身清除率比成人增加30%多、消除半衰期縮短24%。無專門的6歲以下兒童藥代動力學研究。在323例(181例1~5歲兒童、18例6~11歲兒童、124例18~55歲成人)、單次或多次服用1.25~30mg左西替利嗪的受試者進行群體藥代動力學分析,數據顯示6個月~5歲兒童每日一次、每次服用1.25mg所得血藥濃度與成人每日一次、每次服用5mg所得的相似。
腎功能不全:左西替利嗪在輕、中、重、末期腎功能不全患者的暴露量(AUC)與健康受試者的相比,分別增加1.8、3.2、4.3和5.7倍。半衰期預估相應分別增加1.4、2.0、2.9和4倍。口服后左西替利嗪的全身清除率與肌酐清除率相關,根據腎功能的嚴重程度逐步減少。因此推薦根據輕、中、重度腎功能不全患者的肌酐清除率調整劑量和給藥間隔。末期腎功能疾病患者不推薦使用左西替利嗪。左西替利嗪經標準4小時透析程序清除量不超過10%。輕度腎功能不全者應減少左西替利嗪服用量,中或重度腎功能不全者的劑量及給藥頻率也同樣需減少。(見【用法用量】)。
肝功能不全:未在肝功能不全患者研究左西替利嗪。健康受試者口服給藥后的非腎清除(預示肝功能正常)約占全身清除率的28%。因左西替利嗪主要以原形經腎消除,僅肝功能不全者不可能明顯降低左西替利嗪的清除。
【貯藏】
密閉,不超過25℃保存。
【包裝】
口服液體藥用聚酯瓶,每瓶150ml,每盒1瓶。配備有帶刻度的量杯。
【有效期】
18個月。
開封后需在3個月內服用,逾期廢棄。
【執行標準】
YBH00392022
【批準文號】
國藥準字H20223049
【藥品上市許可持有人】
企業名稱:北京柏雅聯合藥物研究所有限公司
地 址:北京市豐臺區科技園富豐路4號10A04-01
郵政編碼:100070
電話號碼:010-61264668
網址:www.gftsg.cn
【生產企業】
企業名稱: 廣東眾生藥業股份有限公司
地 址: 廣東省東莞市石龍鎮西湖工業區信息產業園
郵政編碼: 523325
電話號碼: 0769-86100111






